
石家庄鑫富达医药包装有限公司是专业生产塑料包装的知名企业,公司从业二十余年,以精湛的技术、完善的管理体系、精益求精的产品服务于广大客户。产品远销到亚洲、欧洲、南北美洲等地区。是中国兽药协会理事单位,受农业部(农业农村部)委托参与制定兽药包装团体标准。富于厚德,达于至善。
查看详情兽用预灌封塑料乳房注入器
1 范围
本标准规定了兽用预灌封塑料乳房注入器的术语和定义、产品分类、技术要求、特性指标、试验方法、检验规则、标识、包装、运输和贮存。
本标准适用于兽用子宫灌注剂、兽用乳房灌注剂的包装。
本标准适用于以聚乙烯(PE)、聚丙烯(PP)为主要原料,采用注塑工艺生产的塑料预灌封。
2 规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。GB/T2828.1-2012 计数抽样检验程序 第1部分:按接收质量限(AQL)检索的逐批检验抽样计划YBB00112004-2015 预灌封注射器组合件(带注射针)YBB00092002-2015 口服液体药用高密度聚乙烯瓶《中华人民共和国兽药典》2015版《中华人民共和国药典》2015版
3 术语和定义
下列术语和定义适用于本标准。
3.1 兽用预灌封塑料乳房注入器
兽用预灌封塑料乳房注入器组件由针管、管帽、推杆或加活塞组成,各塑料组件均采用注塑工艺生产。
4 产品分类
4.1 产品按规格分类
1ml -100ml 也可根据客户要求定制。
5 技术要求
5.1 原料
各组件主要原料为聚丙烯(PP)或聚乙烯(PE)。
5.2 外观质量
外观质量要求应符合表1的规定。
表1 外观质量要求

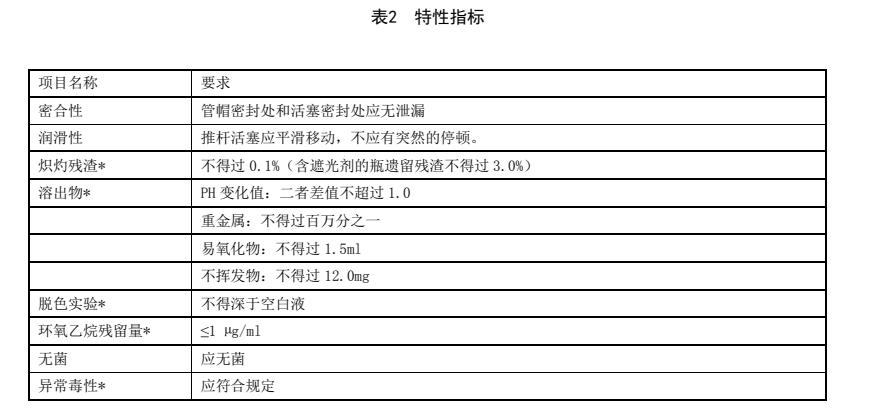
5.3 特性指标
特性指标应符合表2的规定。
6 试验方法
6.1 试验条件
6.3 密合性
取本品适量,在针管中加一半的水(或有色溶液),配好推杆赶出空气,确保其中无空气,戴好护帽,通过推杆,在推杆活塞上面施加轴向压力30N,保持30秒,护帽密封处和活塞密封处应无泄漏。
6.4 润滑性
取本品适量,将推杆(加活塞的推杆)插入针管中,将推杆推入整个针管中,推杆活塞应平滑移动,不应有突然的停顿。
6.5 炽灼残渣*
取针管 2.0g,依法测定(《中华人民共和国兽药典》2015年版二部通则0841),遗留残渣不得过0.1%(含遮光剂的瓶遗留残渣不得过3.0%)。
6.6 溶出物*
供试液的制备:分别取本品(针管)内表面积600cm2(分割成长 5cm ,宽 0.3cm 的小片),置具塞锥形瓶中,加水适量,振摇洗涤小片,弃去水,重复操作二次。在 30~40℃干燥后,用水(70℃±2℃)200ml 浸泡24小时后,取出放冷至室温,用同批试验用溶剂补充至原体积作为供试液,以同批水为空白液,进行下列试验 :
6.6.1 pH 变化值
取水供试液与水空白液各20ml,分别加入氯化钾溶液(1→1000)1.0ml,依法测定(《中华人民共和国兽药典》2015年版二部通则0631)测定,二者pH值之差不得过1.0。
6.6.2 重金属
精密量取水供试液20ml,加醋酸盐缓冲液(pH 3.5) 2ml,依法测定(《中华人民共和国兽药典》2015年版二部通则0821第一法),含重金属不得过百万分之一。
6.6.3 易氧化物
精密量取水供试液20ml,精密加入高锰酸钾滴定液(0.002mol/L)20ml与稀硫酸1ml,煮沸3分钟,
迅速冷却至室温。加0.1g碘化钾,在阴暗处放置5分钟,用硫代硫酸钠滴定液(0.01mol/L)滴定,滴定至近终点时,加入淀粉指示液5滴,继续滴定至无色。另取水空白液同法操作,二者消耗硫代硫酸钠滴定液(0.01mol/L)之差不得过1.5ml。
6.6.4 不挥发物
精密量取水供试液和空白液各50ml,分别置于已恒重的蒸发皿中,水浴蒸干,105℃干燥至恒重,两者之差不得过12.0mg。
6.7 脱色实验*
(适用于着色针管)取本品适量,截取针管表面积50 cm2(以内表面积计)三份,剪成2cm×0.3cm的小片,分别置于3个具塞锥形瓶中,分别加入4%醋酸溶液(60℃ ±2℃)、65%乙醇(25℃±2 ℃)、正己烷(25℃±2 ℃)水浴中恒温2小时后,取出放冷至室温,以同批4%醋酸溶液、65% 乙醇、正己烷为空白液,浸泡液颜色不得深于空白液。
6.8 环氧乙烷残留量*
样品制备:取本品除去包装,吸入标示容量(V)的蒸馏水,在37℃±1℃的条件下平衡1小时。对照贮备液制备:取外部干燥的50ml容量瓶,加水30ml,加瓶塞,称重,精确到0.1mg。用注射器注入0.6ml环氧乙烷对照品(纯度大于99.7%),轻轻摇匀,再盖好瓶塞,称重,两次称重之差即为环氧乙烷重量。加水至刻度再将此溶液稀释成1g/L作为对照贮备液。在稀释成环氧乙烷含量为1µg/ml的溶液,作为对照液。
将对照液和样品各取5ml置顶空瓶,分别置于60℃±1℃的条件下平衡20分钟。分别取1ml液上气体注入气象色谱仪中,记录色谱图,测量对照品和样品的峰面积。对照液的峰面积应大于样品的峰面积。环氧乙烷残留量应≤1µg/ml。
6.9 无菌
(灭菌后)取本品适量,加入1/2 标示容量的氯化钠注射液,盖好活塞和管帽,振荡1分钟,合并提取液。取提取液接种硫乙醇酸盐流体培养基(TG)小管(每管9ml)2只,每管0.2ml;一只置35~37℃培养,一只置23~25℃培养。另用一只TSB小管(每管7ml)接种0.2ml,置23~25℃培养,照无菌检查法(《中华人民共和国兽药典》2015年版三部附录3306)检查,应符合规定。
6.10 异常毒性*
取本品数只,针管用水清洗干净后,剪碎,取500cm2(以内表面积计),加入氯化钠注射液50ml,置高压蒸气灭菌器110℃保持30分钟后取出,冷却后备用,以同批氯化钠注射液做空白,静脉注射,依法检查(《中华人民共和国兽药典》2015年版二部通则1111),应符合规定。
7 检验规则
7.1 检验分类
产品检验分为出厂检验、型式检验、监督检验。
7.2 型式检验
7.2.1 在有下列情况之一时,应进行型式检验:
a) 新产品备案;
b) 产品出现重大质量事故后,重新生产;
c) 监督抽验;
d) 产品停产后,重新恢复生产;
e) 每年至少进行一次型式检验;
f) 带*项目半年内至少检查一次。
7.2.2 型式检验项目应包括外观质量、特性指标。
7.3 出厂检验
7.3.1 每批产品经制造商质量检验部门检验合格,并附产品合格证后方能出厂。
7.3.2 出厂检测项目按 6.2/6.3/6.4/6.9 的要求进行产品检验,检验项目包括外观质量、特性指标等。
7.3.3 按 GB/T 2828.1-2012 中正常检查一次抽样方案进行,检验项目、接收质量限 AQL 级检验水平见

7.3.4 检验结果中,按照计数抽样检验程序第 1 部分:按接收质量限(AQL)检索的逐批检验抽样计划
(GB/T2828.1-2012)判定密封性不合格的,则判为不合格;其他项目中如有不合格的,允许加倍抽样
对不合格项目进行复检,如复检仍有不合格项,则判该批产品为不合格。
7.4 监督检验
监督检验时国家质量监督机构按照规定对生产厂家进行抽样检验的活动。
7.5 检验批
用具有同一性质、质量和同一配方,并在同一连续生产周期中生产出来的一定数量的产品为一批。
8 标识、包装、运输、贮存
8.1 标识
每个产品的小包装上应有下列标志:
a) 产品名称及商标;
b) 厂名和厂址;
c) 批号、型号规格;
d) 执行标准编号;
e) 生产日期;
f) 产品大包装上除应有以上的标志外,还应标明数量,“怕雨”﹑“怕晒”﹑“堆码层数极限
N=8”等标志应符合 GB/T 191-2008 的有关规定。
8.2 包装
纸箱做外包装,塑料袋做内包装,置干燥通风处保存。
8.3 运输
运输中应注意防晒,防雨雪。不得与有毒或有害物品混合运输。
8.4 贮存
贮存环境要求应为干燥、通风良好的室内,周围无有害或腐蚀性物品。
复验期:24 个月。
原文下载: