
石家庄鑫富达医药包装有限公司是专业生产塑料包装的知名企业,公司从业二十余年,以精湛的技术、完善的管理体系、精益求精的产品服务于广大客户。产品远销到亚洲、欧洲、南北美洲等地区。是中国兽药协会理事单位,受农业部(农业农村部)委托参与制定兽药包装团体标准。富于厚德,达于至善。
查看详情动物疫苗复合皂苷佐剂(YSKM101)
1、范围
本标准规定了动物疫苗复合皂苷佐剂(YSK MI01)的质量要求、用法用量、检验方法、检验规则、标签、包装、运输、贮存及保存期。
本标准适用于动物疫苗复合皂苷佐剂(YSK M101)的加工、贮存和使用。
2、规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅所注日期的版本适用于本文件,凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
《中华人民共和国兽药典(2020年版)》、《中华人民共和国药典(2020年版)》:生产和检定用设施、原材料及辅料、注射用水、器具等应符合本有关规定要求。
GBIT 191-2008 包装储运图示标志:动物疫苗复合皂苷佐剂(YSK M101)的包装储运图示标志的名称、图形符号、尺寸、颜色及应用方法应符合本规定要求。
3、术语和定义
下列术语和定义适用于本标准。
3.1 佐剂
佐剂(Adiuvant)是一种先于抗原或与抗原混合后同时注入动物体内,能非特异性的改变或增强机体对抗原的免疫应答,发挥增强免疫效果的物质。疫苗佐剂可以通过增加抗表面积,延长抗原在体内的驻留时间,增强抗原递呈细胞的呈递效率,刺激淋巴细胞的增殖分化等作用,来提高疫苗的保护效果,延长疫苗的保护期等。
3.2 皂普
皂苷(Saponin),是螺旋甾烷类化合物或三萜的天然糖苷,能够表现出不同的生物学和药理活性,对哺乳动物的免疫系统具有激活作用。
最广泛使用的基于皂苷的佐剂是OuilA及其衍生物OS-21,皂佐剂不仅可以促进T、B淋巴细胞增殖,提高NK细胞的杀伤活性,增强巨细胞吞能力等,提高动物机体对抗原的特异性抗体水平:而且还可诱导产生特异性MHC-I抗原限制性CTL,并刺激分泌多种细胞因子,如IL-10、IL-4、IFN-Y、TNF-a等。皂苷作为疫苗佐剂,能够增强免疫刺激作用,在动物疫苗中已经广泛使用。对于抗病毒、抗肿瘤等新型疫苗,不同种类的皂苷及其衍生物有着良好的佐剂效应,因此新型皂苷佐剂的研究对于现代疫苗的开发有着重要作用。
4 略语
下列缩略语适用于本标准。
pH:酸碱度(pondus hydrogenii )
mg:毫克(milligram)
ml:毫升(milliliter)
EU:内毒素活性单位(Endotoxin Unit)
mpm:转/每分(revolutions per minute)
min:分钟(minute)
w:质量(wcight)
L:升(liter)
'℃:摄氏度(degrce celsius)
5 质量要求
5.1 基本要求
生产和检定用设施、原材料及辅料、注射用水、器具等应符合《中华人民共和国兽药典(2020年版)》、《中华人民共和国药典(2020年版)》的有关要求。
5.2 制备
取一定量的皂苷和注射用水投入配液罐,以100-200rpm混合均匀后,加入多糖、增溶剂,再次以100-200mpm混合均匀后过滤除菌,分装即得动物疫苗复合皂苷佐剂(YSK M101)。
5.3 性状
淡黄色或琥珀色澄清透明液体。
5.4技术指标
技术指标及质量应符合表1的要求
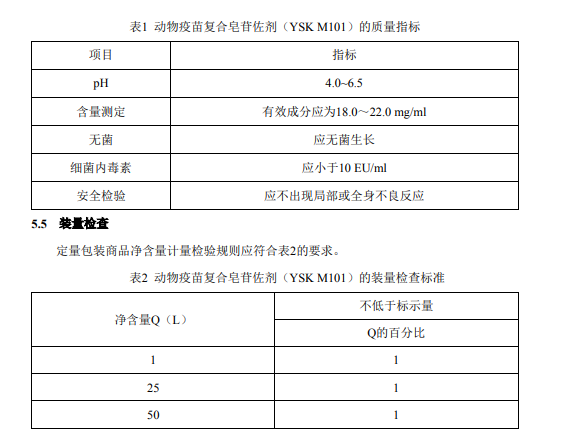
6、用法用量
适用于猪、牛、羊等动物用灭活疫苗、亚单位疫苗和合成肽疫苗。猪等动物推荐佐剂与抗原以1:199(w/w)比例使用:配苗时在室温下采用120mpm转速搅拌5-10min。本品为无菌产品,可直接使用。
7 、检验方法
7.1 性状检验
取本品适量,在无色透明容器内,在自然光条件下,目测其外观应为淡黄色或琥珀色澄清透明液体。
7.2 pH测定
取本品适量,依法检查(《中华人民共和国兽药典(2020年版)(三部)》附录3101),pH值应为4.0-65.
7.3 含量测定
取本品适量,依法检査(《中华人民共和国兽药典(2020年版)(一部)》附录0512),有效成分应为18.0-22.0 mg'ml。
7.4 无菌检验
取本品适量,依法检査(《中华人民共和国药典(2020年版)(四部)》通则1101),应无菌生长。
7.5 细菌内毒素测定
取本品适量,依法检测(《中华人民共和国兽药典(2020年版)(一部)附录1143》),细菌内毒素应小于10 EU/ml。
7.6 安全检验
14--21日龄健康仔猪,随机分为生理盐水对照组与试验组,每组5头。生理盐水对照组每头肌肉注射无菌生理盐水2.0ml。试验组每头肌肉注射复合皂苷佐剂疫苗2.0ml。每日定时测定体温,观察14日。试验动物应未出现局部或全身不良反应,
8 检验规则
8.1 组批
以相同材料、相同生产工艺、连续生产或同一班次生产的产品为一批。
8.2 采禅
采样按《兽药质量监督抽样规定》的规定执行。
8.3 出厂检验
8.3.1 出厂检验项目
出厂检验项目为:性状、pH测定、含量测定、无菌检验、细菌内毒索测定等指标进行检验,合格后发出合格证方可出厂。
8.3.2 判断方法
所检项目检测结果均符合本标准规定指标判定为合格产品。
检验结果中如有一项指标不符合本标准规定时,可在原批中重新抽样对不符合项进行复验,若复验结果仍不符合本标准规定,则判定该批产品为不合格。
8.4.1 型式检验项目为第5章规定的全部项目。
8.4.2 产品正常生产时,每半年至少进行一次型式检验,但有下列情况之一时,应进行型式检验:
a)改变配方或生产工艺:
b)原料、设备、加工工艺有较大改变时:
c)产品停产3个月以上,恢复生产时:
d)出厂检验结果与上次型式检验结果有较大差异时:
c)当兽药管理部门提出进行型式检验要求时。
8.4.3 判定方法
所检项目检测结果均与本标准规定指标一致判定为合格产品。
所检结果中如有一项指标不符合本标准规定时,可在原批中重新抽样对不符合项进行复验,若复验结果仍不符合本标准规定,则判定该批产品为不合格,
9 标签、包装、运着、贮存、保存期
9.1 标签
标签内容包括:产品名称,规格,用量用法,生产批号,生产日期,有效期,生产厂家,地址,电话等。
9.2 包装
1 L/瓶、25 L/桶、50 L桶。
包装材料符合国家药品包装材料卫生标准的要求。封口严密,包装牢固。产品用塑料瓶、桶进行包装。
9.3 运输
2-8“℃冷链运输。
贮存。4
2-8°℃避光保存。
保存期非与
在符合标准规定的包装、运输、贮存条件下,保存期为2年。
来源:兽药协会
原文下载;![]() 1-240R1100005.pdf
1-240R1100005.pdf